Pengertian & perbedaan Atom, Molekul, Ion, Unsur, Senyawa, Campuran
PARTIKEL PENYUSUN MATERI/ZAT
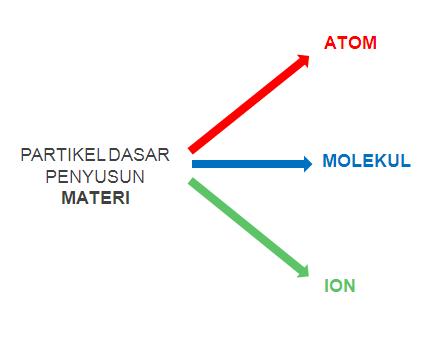
Partikel adalah sebuah satuan dasar dari benda atau materi. Bisa juga dikatakan Partikel merupakan satuan bagian terkecil dari suatu materi. Jenis Partikel ini ada 3 yaitu: atom, molekul, dan ion. Jadi baik atom, molekul, dan ion ke tiga-nya merupakan satuan terkecil dari materi yg secara umum disebut partikel
1. Atom adalah: Satuan terkecil dari suatu materi yang terdiri atas inti, yang biasanya mengandung proton (muatan+) dan neutron (netral), dan kulit yang berisi muatan negatif yaitu elektron. Ada juga yang menyebutkan bahwa atom adalah partikel penyusun unsur.
Kedua pengetian ini semuanya benar. Yang pasti atom itu :
– punya proton, neutron, elektron, (kecuali pd Hidrogen-1, yg tidak memiliki neutron)
– punya karekteristik tertentu, yaitu punya jumlah proton dan elektron yang sama (jika tdk sama disebut ion)
– atom2 yang punya karakteristik yang sama dinamakan unsur,
Analogi sederhana: Setiap orang yang sering membaca, kita sebut sikutu buku, ceritanya kita punya 4 teman yang punya hobi membaca, sehingga kita simpulkan keempat teman kita ini sikutubuku karena punya kebiasaan yang sama. Jadi
teman kita= atom,
sama2 hobi baca= punya jumlah proton&elektron sama/ berkarakter sama,
sikutu buku=unsur
Anggapan yang salah
– gabungan/ikatan beberapa atom akan membentuk unsur (SALAH).
Yang benar: unsur adalah nama untuk kumpulan/himpunan atom yang punya karakter yang sama. Gabungan/ikatan dari beberapa atom bukan membentuk unsur tapi membentuk molekul. Bedakan himpunan dan ikatan..!
2. Molekul adalah: Gabungan dari beberapa atom unsur, bisa dua atau lebih. Artinya ketika berbicara molekul maka yang dibayangkan adalah gabungan atom2 (bukan 1 atom). Molekul adalah partikel terkecil dari suatu unsur/senyawa
– Jika gabungan dari atom unsur yang sama jenisnya maka disebut Molekul Unsur, Contohnya: O2, H2, O3, S8
– Jika gabungan dari atom unsur yang berbeda jenisnya maka disebut Molekul Senyawa, Contohnya: H2O, CO2, C2H5
3. Ion adalah: atom yang bermuatan listrik, ion yang bermuatan listrik disebut kation, dan ion yang bermuatan negatif disebut anion. Kation dan anion dapat berupa ion tunggal hanya terdiri dari satu jenis atom atau dapat pula berupa ion poliatom mengandung dua atau lebih atom yang berbeda.
Beberapa Kesimpulan:
Unsur itu partikelnya bisa berupa atom/molekul unsur. Unsur2 yang partikelnya berupa atom, berarti unsur tersebut bisa berdiri sendiri atau hanya mengandung satu atom saja, penulisannya ditulis dengan lambang unsurnya, misalnya C (karbon), He (Helium). Bila partikelnya berupa molekul maka artinya unsur tersebut dibentuk dari gabungan atom yang berjenis sama, dia tidak bisa berdiri sendiri, unsur2 tersebut ditulis dengan lambang unsurnya disertai dengan jumlah atom penyusunya. Contohnya: O2, H2. Makanya unsur oksigen tidak pernah ditulis hanya huruf O saja, melainkan ditambah angka 2 sebagai arti bahwa Unsur ini dibentuk dari 2 atom oksigen.
JENIS-JENIS MATERI/ZAT
Materi/Zat secara umum dibagi menjadi 2 bagian yaitu zat tunggal dan campuran. Zat tunggal dapat berupa unsur, atau berupa senyawa. Sedangkan campuran dapat berupa campuran homogen atau berupa campuran heterogen.
1. Unsur adalah: Sekelompok atom yang memiliki jumlah proton yang sama pada intinya. Jumlah ini disebut sebagai nomor atom unsur. Unsur didefinisikan pula sebagai zat tunggal yang sudah tidak bisa dibagi-bagi lagi menjadi bagian yang lebih kecil.
Saya hanya ingin menekankan “unsur hanyalah sebutan saja untuk atom-atom yg yang punya karakter sama (punya jumlah proton yg sama)”. Sebagai contoh, semua atom yang memiliki 6 proton pada intinya adalah atom dari unsur kimia karbon, dan semua atom yang memiliki 92 proton pada intinya adalah atom unsur uranium.
Bisa dibilang unsur adalah atom itu sendiri, contohnya: jika ada H2O, maka kita bisa bilang: terdiri dari 2 atom hidrogen, dan 1 atom oksigen, padahal Hidrogen dan oksigen keduanya adalah unsur.
2. Senyawa: Senyawa adalah zat tunggal yang terdiri atas beberapa unsur yang saling kait-mengait. Senyawa dibentuk dari minimal 2 unsur yang berbeda. Walaupun dibentuk dari unsur yang berbeda, namun senyawa tetap disebut zat tunggal, karena sifat-sifat unsur yang membentuknya tidak dapat di temukan pada senyawa. Dengan kata lain
Senyawa telah menjelma menjadi zat yang baru.
Contoh:
Reaksi antara Hidrogen(H) dan oksigen (O2), diperoleh zat baru yang disebut air, yaitu:
Reaksi antara Hidrogen(H) dan oksigen (O2), diperoleh zat baru yang disebut air, yaitu:
H + O2 ——–> H2O
Pada reaksi tersebut, dihasilkan zat baru yang sifatnya berbeda dari unsur-unsur penyusunnya. Hidrogen adalah gas yang sangat ringan dan mudah terbakar, sedangkan oksigen adalah gas yang terdapat di udara yang sangat diperlukan tubuh kita untuk pembakaran. Tampak jelas bahwa sifat air berbeda dengan sifat hidrogen dan oksigen.
Ciri khas senyawa adalah dia mempunyai perbandingan massa penyusun yang tetap, air tersusun dari oksigen dan hidrogen dengan perbandingan massa unsur oksigen banding hidrogen adalah selalu 8 : 1
Perbedaan Senyawa dan molekul
“setiap senyawa adalah molekul namun setiap molekul belum tentu senyawa”. Senyawa adalah gabungan minimal 2 atom berbeda, sedangkan molekul gabungan minimal 2 atom bisa sama bisa juga berbeda.
3. Campuran: Zat yang tersusun dari beberapa zat yang lain jenis dan tidak tetap susunannya dari unsur dan senyawa. Campuran merupakan materi yang terdiri dari dua atau zat tunggal. Materi yang kita jumpai sehari-hari hampir semuanya campuran. Bahkan kita sering membuat campuran bahan, misalnya ketika kita membuat kopi atau teh manis.
Campuran dibedakan menjadi tiga jenis, yaitu:
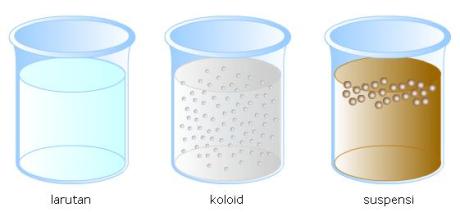
- Campuran homogen = Larutan
- Campuran Heterogen = Suspensi, dan
- Campuran yang keadaannya antara suspensi dan larutan = Koloid
3.1. Larutan adalah: campuran dua zat atau lebih yang terdiri dari zat terlarut dan pelarut. Ukuran partikel larutan sangat kecil, kurang dari 1 nm, sehingga tidak dapat dilihat dengan menggunakan microskop ultra sekalipun. dan tidak dapat dibedakan antara zat terlarut dan medium pelarutnya. Zat dalam larutan tidak dapat dipisahkan melalui penyaringan.
Contoh larutan gula, kita tidak bisa membedakan mana gula mana air dalam larutan gula. Beberapa contoh larutan adalah larutan garam, larutan asam basa dan lain-lain.
3.2. Suspensi adalah: Suspensi adalah campuran kasar dan bersifat heterogen. Ukuran partikel suspensi lebih dari 100 nm.
Contoh suspensi adalah campuran terigu dalam air, apakah masih tampak terigu tersebut ? Jawabannya Ya, Masih. Campuran ini awalnya tampak seperti larutan yang keruh, tetapi lambat laun terpisah karena pengaruh gravitasi (mengalami pengendapan). Suspensi dapat dipisahkan melalui penyaringan. Contoh suspensi yang lain misalnya kapur dengan air, tanah dengan air, es cendol, campuran batu kali dengan pasir dan lain-lain.
3.3. Koloid adalah: Koloid adalah campuran yang terdiri dari partikel terdispersi dan pertikel pendispersi. Ukuran partikel koloid terletak antara 1 nm – 100 nm. Atau dengan kata lain ukuran partikel koloid keadaannya antara suspensi dan larutan.
Contoh koloid adalah air susu, santan, air sabun, dan cat. Koloid tampak keruh tetapi stabil (tidak memisah/mengendap). Bahan dalam campuran koloid tidak dapat dipisahkan melalui penyaringan biasa, melainkan dengan menggunakan penyaring ultra.
Beberapa contoh koloid yang lain adalah susu, buih, santan, agar-agar, mutiara, gelas berwarna dan lain-lain
sumber:









Tidak ada komentar: